上海交通大学附属中学 第二学期高中二年级化学摸底试题
可可以用到的相对原子水平:H-1 O-16 S-32 Na-23 C-12 Ba-137 N-14 Al-27
1、选择题
1. 今年垃圾分类已经立法,有益于资源充分借助,下列处置错误的是( )
A. 厨房菜蔬与残羹收购处置后作肥料
B. 旧报纸等废纸收购再生产纸
C. 电池等电子商品有毒需特殊处置
D. 塑料袋等白色垃圾掩埋处置
2. 下列表示甲基的电子式中,正确的是( )
A. ![]()
![]() B.
B. ![]() C. D.
C. D. ![]()
3. 工业上获得很多乙烯的办法是( )
A. 乙醇脱水 B. 石油分馏 C. 石油裂化 D. 石油裂解
4. 对于有机 ![]() 的命名正确的是( )
的命名正确的是( )
A. 2—乙基戊烷 B. 2—丙基丁烷
C. 2—甲基—3—乙基丁烷 D. 3—甲基己烷
5. 大方污染物氟里昂—12 的化学式是 CF2Cl2,下面关于氟里昂—12 的说法正确的是( )
A. 没固定的熔沸点 B. 分子中的碳原子是饱和的
C. 是正四面体的空间结构 D. 是甲烷的一种同系物
6. 下列元素的单质,工业上一般不用电解法制取的是( )
A. 钠 B. 铝 C. 铁 D. 氯
7. 有一种军用烟幕弹中装有 ZnO、Al 粉和 C2Cl6,其发烟过程中的化学反应如下:
①3ZnO+2Al→Al2O3+3Zn ②3Zn+C2Cl6→3ZnCl2+2C 下列有关叙述不正确的是( )
A. 反应①是铝热反应 B. 反应②是置换反应
C. C2Cl6 是卤代烃 D. 烟幕是小液滴分散在空气中形成的
8. 下列物质可以用化合反应直接制得的是( )
①FeCl2 ②Fe3 ③NaHSO3 ④Fe2
A.② B. ②③ C. ①②③ D. ①②③④
9. 下图是一种形状酷似一条小狗的有机物,化学家 Tim Rickard 将它起名字为“doggycene”,有关 doggycene
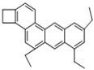 的说法正确的是( )
的说法正确的是( )
A. 该有机物是苯的同系物
B.“doggycene”可以使溴水褪色
C. 该物质常温下为气态
D. 1mol 该物质在氧气中完全燃烧生成 CO2 和水物质的量之比为 2:1
10. 右图是元素周期表的一部分,下列说法中正确的是( )
A. 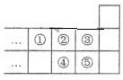 元素①坐落于第二周期ⅣA 族
元素①坐落于第二周期ⅣA 族
B. 气态氢化物的稳定性:④>②
C. 最高价氧化物对应水化物酸性:⑤>④
D. 元素的最高正化合价:③=⑤
11. 某有机物的分子式为 C7H15Cl,若它的消去产物共有 3 种单烯烃,则该有机物的结构简式可能是( )
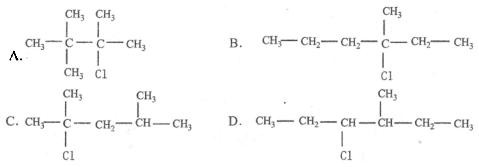 |
12. 用相对分子水平为 43 的烷基取代甲苯上的一个氢原子,所得芳香烃产物的数目为( )
A. 3 种 B. 4 种 C. 6 种 D. 8 种
13. 在 5mL 0.1mol/LKI 溶液中滴加 0.1mol/LFeCl3 溶液 5~6 滴后,生成 Fe2+和 I2,再进行下列实验,其中可证明 FeCl3 溶液和 KI 溶液的反应是可逆反应的实验是( )
A. 在滴加 AgNO3 溶液,察看是不是有 AgI 沉淀产生
B. 加入 CCl4 振荡后,察看下层液体颜色
C. 加入 CCl4 振荡后,取上层清液,滴加 AgNO3 溶液,察看是不是有 AgCl 沉淀产生
D. 加入 CCl4 振荡后,取上层清液,滴加 KSCN 溶液,察看是不是有血红色
14. 下列说法正确的是( )
A. Ⅰ A 族元素的金属性肯定比Ⅱ A 族元素的金属性强
B. 失电子能力弱的元素得电子能力未必强
C. 同主族元素单质的熔沸点从上到下渐渐升高
D. 第三周期主族元素的离子半径,从左到右渐渐减小
15. 肯定能在溶液中很多共存的离子组是( )
A. ![]() 含有很多 Al3+的溶液:Na+、NH4+、SO4 、Cl
含有很多 Al3+的溶液:Na+、NH4+、SO4 、Cl
B. ![]() c=1×10-13 mol/L 的溶液:Na+、Ca2+、SO4 、CO3
c=1×10-13 mol/L 的溶液:Na+、Ca2+、SO4 、CO3
C. ![]() 含有很多 Fe3+的溶液:Na+、Mg2+、NO3 、SCN
含有很多 Fe3+的溶液:Na+、Mg2+、NO3 、SCN
D. ![]() 含有很多 NO3 的溶液:H 、Fe 、SO4 、Cl
含有很多 NO3 的溶液:H 、Fe 、SO4 、Cl
16. ![]() b--月桂烯的结构如右图所示,一分子该物质与两分子溴发生加成反应的产物(只考虑地方异构)理论上最多有( )
b--月桂烯的结构如右图所示,一分子该物质与两分子溴发生加成反应的产物(只考虑地方异构)理论上最多有( )
A. 4 种 B. 6 种 C. 8 种 D. 9 种
17. 在 120℃时,将下列各组烃以任意比率混合,与过量 O2 在一密闭容器中完全反应,测知反应前后的压强没变化,则该混合烃是( )
A. CH4 和 C2H4 B. CH4 和 C2H6 C. C2H2 和 C2H6 D. C3H4 和 C3H6
18. 下列实验设计可以成功的是( )
A. 检验 Na2O2 试样是不是变质为 Na2CO3:向试样中加入盐酸,产生无色无味的气体
B. 检验某卤代烃是不是是氯代烃:
![]() 试样 ¾氢¾氧¾化钠¾溶液¾®冷却 ¾稀¾硫¾酸至¾酸性¾® ¾硝¾酸¾银溶¾液® 出现白色沉淀
试样 ¾氢¾氧¾化钠¾溶液¾®冷却 ¾稀¾硫¾酸至¾酸性¾® ¾硝¾酸¾银溶¾液® 出现白色沉淀
C. 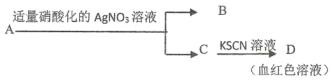 除去溴乙烷中混有些溴:混合液 ¾饱¾和¾碳酸¾钠溶¾液® ¾振¾荡¾® 溶液分层 ¾分¾液¾® 得下层
除去溴乙烷中混有些溴:混合液 ¾饱¾和¾碳酸¾钠溶¾液® ¾振¾荡¾® 溶液分层 ¾分¾液¾® 得下层
D. 鉴别盐 A 的成分是 FeBr2:
19. 已知 Mg2C3 的结构与 CaC2 相似,由此可判定 Mg2C3 与水反应的产物是( )
A. Mg2 和 CH ºCH B. MgO 和 CH ºCH
C. Mg2 和 CH3CH=CH2 D. Mg2 和 CH3C ºCH
20. 几种短周期元素的原子半径及主要化合价见下表:
元素代号 | K | L | M | Q | R | T | N |
原子半径/nm | 0.183 | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.152 |
主要化合价 | +1 | +2 | +3 | +6 | +2 | -2 | +1 |
下列叙述正确的是( )
A. K、L、M 三元素的金属性渐渐增强
B. 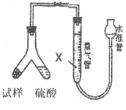 在 RCl2 分子中,各原子均满足 8 电子的稳定结构
在 RCl2 分子中,各原子均满足 8 电子的稳定结构
C. Q 元素的最高价氧化物为电解质,其水溶液可以导电
D. K 在 T 单质中燃烧所形成的化合物中含有非极性共价键和离子键
2、综合剖析题
(一)已知:W、X、Y、Z、T 均为短周期元素,且原子半径依次增大。请填空:
21. W、Z 是形成化合物类型最多的两种元素,写出 Z 的核外电子的轨道表示式
____________________。
22. 化合物 YW3 溶于水能使酚酞变红,用方程式表示酚酞变红是什么原因____________________。
23. 元素 T 的原子中电子占据 7 根轨道,则 T 在元素周期表____________________周期____________________族;
T 的化合物 TY 熔融时不导电,常用作砂轮与耐高温材料,由此推知,它是____________________。
a. 离子晶体 b. 原子晶体 c. 分子晶体 d. 没办法判断
24. YX3 与 YW3 具备相同的分子空间构型,YX3 是____________________(填“极性”、“非极性”)分子,其中 Y 的化合价为____________________。
(二)为测定碳酸氢钠纯度(含有少量氯化钠),学生设计了如下几个实验策略(每一个策略均称取 m1g 样品),请回答每一个策略中的问题。
【策略Ⅰ】使用重量法进行测定:可用下图中的装置进行实验。
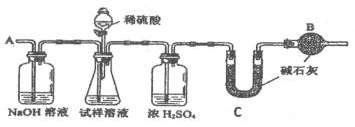 |
25. A 装置中 NaOH 溶液有哪些用途是____________________;若直接向试样溶液中鼓入空气会致使实验测定结果
____________________(填“偏高”、“偏低”或“无影响”)。
26. 该策略需直接测定的物理量是____________________。
【策略Ⅱ】使用滴定法进行测定:
27. 称取 m1g 样品,配成 100mL 溶液,取出 20mL,用 c mol/L 的规范 HCl 溶液滴定,消耗体积为 vmL, 则该试样中碳酸氢钠水平分数的计算式为:____________________。
【策略Ⅲ】使用气体体积法进行测定:可用右图中的装置进行实验。
28. 为了减小实验误差,量气管中加入的液体 X 为____________________。
29. 通过实验,测得该试样中碳酸氢钠水平分数偏低,产生这种现象是什么原因可能 是____________________。
a. 测定气体体积时未冷却至室温
b. 测定气体体积时水准管的水面高于量气管的水面
c. Y 型管中留有反应生成的气体
d. 气体进入量气管前未用浓硫酸干燥
【策略Ⅳ】其操作步骤如下:
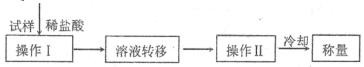 |
30. 操作Ⅱ的名字是____________________。
31. 实验中需要的仪器有电子天平、蒸发皿、玻璃棒等,还需要的玻璃仪器是____________________。
32.  在转移溶液时,如溶液转移不完全,则碳酸氢钠水平分数的测定结果____________________(填“偏高”、“偏低”或“无 影响”)。
在转移溶液时,如溶液转移不完全,则碳酸氢钠水平分数的测定结果____________________(填“偏高”、“偏低”或“无 影响”)。
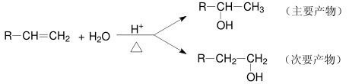
(三)已知:
现以 2-甲基丙烷为有机材料,配以其他必要的无机物材料,选择反应中的主要产物按以下步骤合成商品:
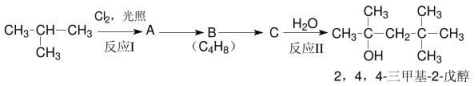 |
请回答:
33. 写出丙烯与氯化氢反应的主要产物的结构简式____________________;
34. 写出反应Ⅰ得到产物可能的结构简式____________________;
35. 写出反应种类:反应Ⅰ____________________、反应Ⅱ____________________;
36. 写出 A→B 的反应条件____________________;B→C 的化学方程式____________________。
(四)某结晶水合物含有两种阳离子和一种阴离子。称取两份水平均为 45.3g 的该结晶水合物,分别制成溶液向其中一份逐滴加入 NaOH 溶液,开始发现溶液中出现白色沉淀并渐渐增多;一段时间后有气体逸出, 该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,加热后共计可采集到 2.24L 该气体(标准情况);最后白色沉淀渐渐降低并最后消失。另一份逐滴加入 Ba2 溶液,开始现象类似,但最后仍有白色沉淀; 过滤,用稀硝酸处置沉淀物,经洗涤和干燥,得到白色固体 46.6g。
请回答以下问题:
37. 该结晶水合物中含有些两种阳离子是____________________和____________________,阴离子是____________________;
38. 试通过计算确定该结晶水合物的化学式。写出计算过程:
假设过程中向该溶液中加入的 Ba2 溶液的物质的量浓度为 2.0mol×L-1 。
39. 加入____________________mLBa2 溶液时,所得沉淀的总物质的量最大。
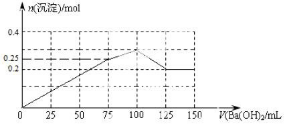
40.
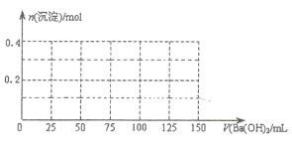 |
请在下图中画出生成沉淀的物质的量与加入 Ba2 溶液体积的关系示意图。
参考答案
1、选择题
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
D | C | D | D | B | C | D | C | D | C |
11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
B | C | D | B | A | A | A | C | D | D |
2、综合剖析题
(一)21. ![]()
22. ![]() NH3+H2O⇌ NH3∙H2O⇌ NH4 +OH
NH3+H2O⇌ NH3∙H2O⇌ NH4 +OH
23. 三;IIIA;b
24. 极性;+3
(二)25. 吸收空气中的 CO2;偏高
26. 装置 C 反应前后的水平
![]() 27. 0.42cV ´100%
27. 0.42cV ´100%
m1
28. 饱和 NaHCO3
29. b
30. 蒸发
31. 烧杯、酒精灯
32. 偏高
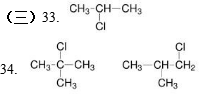 |
35. 取代反应;加成反应
36. 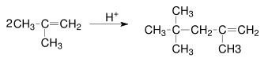 NaOH 醇溶液、加热;
NaOH 醇溶液、加热;
(四)37. NH4+;Al3+;SO42-
38. NH4Al2∙12H2O[或2SO4∙Al23∙24H2O]
39. 100
 40.
40.







