2019 学年第一学期初三阶段测试
化学试题
(满分 60 分,完成时间 40 分钟) 2019.12
相对原子水平:H-1 C-12 O-16
6、选择题(每小题只有一个正确选项,共 20 分)
27.1.下列有关蔗糖的假设是化学变化的是
A.能否溶于酒精 B.能否磨碎变成糖粉
C.能否变成酒精 D.能否通过结晶办法变成大晶体
28.下列物质中,是纯净物的是
A.豆浆 B.酒精 C.食醋 D.牛奶
29.下列物质放入水中,不可以形成溶液的是
A.花生油 B.白糖 C.白酒 D.白醋
30.ClO2 中氯元素的化合价为
A.-1 B.-2 C.+2 D.+4
31.50℃时某物质的溶解度为 100 克/100 克水,则 50℃时此物质的饱和溶液中水平关系为
A.溶质∶溶液=1∶1 B.溶质∶溶剂=1∶1
C.溶剂∶溶液=1∶1 D.饱和溶液的水平肯定为 200 g
32.家庭常用液体的pH如下,酸性最强的是
A.洁厕精:
1.0 B.洗发水:7.6 C.洗衣液:
10.5 D.漂白液:
13.4
33.下列各种原因不会干扰固体溶解度的是
A.溶质的类型 B.溶剂的类型 C.溶剂的水平 D.温度的变化
34.打开汽水瓶盖后会有很多气泡冒出,产生这一现象是什么原因二氧化碳的溶解度随
A.压强增大而减小 B.压强减小而减小 C.温度升高而增大 D.温度减少而减小
35.下列物质在氧气中燃烧,生成物是黑色固体的是
A.木炭 B.铁 C.硫 D.磷
36.用氯化钠固体和蒸馏水配制 50g10%的氯化钠溶液,无需的实验仪器是
A.玻璃棒 B.蒸发皿 C.烧杯 D.天平
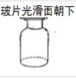

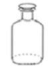
![]() 37.实验室中下列药品存放规范的是
37.实验室中下列药品存放规范的是
A.氧气 B.氢氧化钠溶液 C.硝酸钾固体 D.稀盐酸
38. 下列物质的名字和化学式相对应的是
A.胆矾 CuSO4 B.氯化氨 NH4Cl
C.氢氧化铁 Fe2 D.氧化钙 CaO
39.20℃时,15 g A 与 30 g 水混合正好形成饱和溶液,40℃时,20 g 水最多能溶解 5 g B 物质, 则 A、B 两物质的溶解度大小关系是
A.SA>SB B.SA<SB C.SA=SB D.没办法确定
40.对“水平分数为 10%的食盐水”含义讲解错误的是
A.100g 食盐溶液中溶有 10g 食盐 B.将 10g 食盐溶于 90g 水中所得的溶液
C.100g 水中溶解了 10g 食盐 D.将食盐与水按 1:9 的水平比配成溶液
41.对于某一澄清透明的酸雨样品,判断正确的是
A.呈中性 B. pH>7 C.是悬浊液 D.是溶液
42.室温下,把 100g10%的硝酸钾溶液中溶质水平分数增加到 20%,可以使用的办法是
A.蒸发掉 45g 水 B. 蒸发掉 50g 水
C.加入 10g 硝酸钾 D.加入 100g 10%硝酸钾溶液
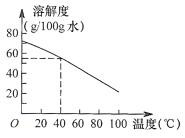 43.某物质的溶解度曲线见右图。
43.某物质的溶解度曲线见右图。
40℃时将 60g 该物质放入 100 g 水 中充分溶解,有关判断正确的是
A.40℃时能形成 160g 溶液
B.若降温至 20℃,溶质水平降低 C.若升温至 60℃,溶质水平分数不变 D.若升温至 80℃,溶液是饱和溶液
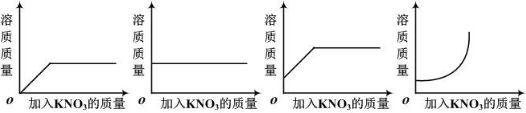 44. 25℃时,向适量不饱和的 KNO3 溶液中渐渐加入 KNO3 固体, 下列图像中能正确表示此过程中溶质水平变化状况的是
44. 25℃时,向适量不饱和的 KNO3 溶液中渐渐加入 KNO3 固体, 下列图像中能正确表示此过程中溶质水平变化状况的是
A. B. C. D.
45.20℃时,恒温蒸发某硝酸钾溶液,首次蒸发掉 10g 水,没晶体析出;第二次又蒸发 掉 10g 水,析出 3 克晶体;第三次再蒸发掉 10g 水,析出 m 克晶体
A.m <3 B.m≤3 C.m>3 D.m≥3
46.右图表示 M、N 两种固体物质的溶解度曲线,下列对图示信息的描述正确的是
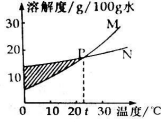 A.30℃时 M 的溶解度小于 N 的溶解度
A.30℃时 M 的溶解度小于 N 的溶解度
B.M、N 都是可溶物质
C.P 点表示 t℃时 M、N 的溶解度相等
D.阴影处各点对应的溶液(不包括曲线上的点)是 M 的 不饱和溶液 ,N 的饱和溶液
7、填空题(共 23 分)
47.化学与生活密切有关,请按需要填空。
![]() ① 用 来 检 验 无 水 酒 精 中 是 否 含 有 水 的 物 质 是 __________________________________________________________________________________________化 学 方 程 式 为
① 用 来 检 验 无 水 酒 精 中 是 否 含 有 水 的 物 质 是 __________________________________________________________________________________________化 学 方 程 式 为
__________________________________________________ ;
② 引起酸雨的主要物质是______________________________________________________________________;
③ 自来水生产过程中加液氯的目的是______________________________________________________________________;
④丙烷(C3H8)是液化石油气的主要成分,C3H8 的摩尔水平是______________________________________________________________________,其中碳元素的 水平分数是______________________________________________________________________(用分数表示),0.25 mol C3H8 中约含有______________________________________________________________________个 H 原子。
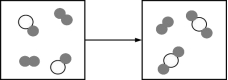 48.走进化学变化的微观世界,有益于进一步认识化学变化。如图是某化学变化的微观示 意图,据图回答问题:
48.走进化学变化的微观世界,有益于进一步认识化学变化。如图是某化学变化的微观示 意图,据图回答问题:
点燃 
①写出反应中氧化物的化学式__________________________________________________;
![]() ②参与反应的
②参与反应的 ![]() 的与 的分子个数比为__________________________________________________;
的与 的分子个数比为__________________________________________________;
③试写出该变化的化学方程式:________________________________________________________________________________;
④该反应的基本反应种类是______________________________________________________________________ 。
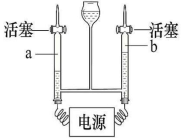 49.用如图装置进行水的电解实验。已知氢氧化钠在水的电解 实验中,只起到增强水的导电性用途。
49.用如图装置进行水的电解实验。已知氢氧化钠在水的电解 实验中,只起到增强水的导电性用途。
①开始反应前 a、b 两管内都充满 4%的氢氧化钠溶液。 关闭活塞,接通电源,可以看到两个电极上出现____________________________________________________________ ; 一段时间后,两管产生的气体如图所示,则 a 管下方导线应接 电源的____________________________________________________________ (填“正”或“负”)极,用____________________________________________________________ 验证 b 管中的气体。
②该实验证明水是由__________________________________________________组成的,电解水的方程式为____________________________________________________________
③ 电解后溶液的溶质水平分数__________________________________________________4%(选填“<”、“=”或“>”)。
![]() 50.下表是 NaCl 和 KNO3 物质在不同温度下的部分溶解度数据(单位:g/100g 水),请回答
50.下表是 NaCl 和 KNO3 物质在不同温度下的部分溶解度数据(单位:g/100g 水),请回答
问题: |
| |||||
| 温度(℃) | 10 | 20 | 30 | 40 | 60 |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.3 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 110 |
① 20℃时,NaCl 的溶解度是______________________________g/100g 水;
③ 以上两种物质溶解度变化受温度影响较小的是________________________________________(选填“NaCl”或“KNO3”);
④20℃时,将 20 g NaCl 固体加入 50 g 水中,充分搅拌,形成的溶液水平为______________________________g;
⑤ 为了将混有少量 NaCl 杂质的 KNO3 的饱和溶液提纯,可通过______________________________办法获得较纯净的
KNO3 晶体;
⑥40℃时,将 NaCl 和 KNO3 的饱和溶液各 100g 降温到 20℃,对剩余溶液描述正确的是
______________________________。
A.溶质的水平分数:NaCl<KNO3 B.析出固体的水平:NaCl>KNO3
C.NaCl 和 KNO3 都是饱和溶液 D.溶剂的水平:NaCl>KNO3
8、简答卷(共 17 分)
51.下图是配制 100g 溶质水平分数为 10% 的 NaCl 溶液实验操作示意图:

A B C D E
①用上图的序号表示配制溶液的正确操作顺序是______________________________;
②图 D 中,取用固体 NaCl 的仪器名字是______________________________;
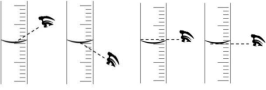 ③图 E 中,将氯化钠放在称量纸上,称出______________________________g 氯化钠;量取所需的水(此时水的密 度可看作 1g/ml),应选择量筒的规格是________________________________________ (选填“l0”、“50”或“100”)ml。量 取读数时,下图视线角度正确的是______________________________(填序号);
③图 E 中,将氯化钠放在称量纸上,称出______________________________g 氯化钠;量取所需的水(此时水的密 度可看作 1g/ml),应选择量筒的规格是________________________________________ (选填“l0”、“50”或“100”)ml。量 取读数时,下图视线角度正确的是______________________________(填序号);
A. B. C. D.
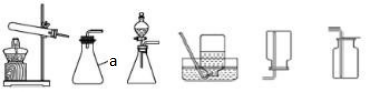 52.依据下面的装置图,回答下列问题:
52.依据下面的装置图,回答下列问题:
A B C D E F
①写出指定仪器的名字:a.______________________________
②用装置 A 作为发生装置制取氧气,发生反应的化学方程式为______________________________,其中二氧化锰的作 用是______________________________;可用 D 装置采集氧气,是由于氧气______________________________的性质,当看到______________________________现象时,说明氧 气收满;
③实验室用溶质水平分数为 20%的过氧化氢溶液和二氧化锰制氧气,并使用图 B 做发 生装置时,同学们发现不可以得到平稳的氧气流,大伙提出从两方面加以改进:
一是使用图 C 做发生装置,其理由是________________________________________;
二是加水稀释过氧化氢溶液,若把 50g 溶质水平分数为 20%的过氧化氢溶液稀释成溶质 水平分数为 5%的过氧化氢溶液,需加水的水平为______________________________g;
④现有一瓶 102g 双氧水,加入适当二氧化锰,完全反应后生成氧气的物质的量为
0.03mol,试计算参与反应的过氧化氢的物质的量和这瓶双氧水溶质水平分数。(写出计算过 程)(13)







